염증성장질환 연구협회 GETAID 주도
램시마SC, 프랑스에 올 2월 출시…처방 확대 박차
프랑스의 염증성장질환(IBD) 연구진들이 셀트리온(대표 기우성)에서 개발한 램시마 정맥주사(램시마IV)와 램시마 피하주사(램시마SC)를 교체 투여하는 연구에 돌입했다.
환자 편의성을 높인 램시마SC로의 교체 투여 연구에서 좋은 결과가 나온다면 현지 처방 확대에 도움이 될 전망이다.
17일 미국 임상등록사이트 클리니컬트라이얼즈에 따르면 프랑스 소재 IBD 연구협회인 GETAID(Groupe d'Etude Therapeutique des Affections Inflammatoires Digestives)가 램시마IV를 램시마SC로 교체 투여한 후 2년 뒤에 효능과 안전성 등이 동일한지 확인하는 임상시험에 돌입했다.
목표 대상자는 프랑스 내의 IBD 환자 총 400명이다. 지난 13일 기준 환자 모집 전인 것으로 파악되고 있다. 예상 모집 시작 일자는 올해 9월, 시험 종료일은 2024년 8월말이 될 것으로 전망된다.
GETAID는 제약사 등 파트너의 도움 여부와 상관없이 독자적으로 연구를 수행하는 기관으로 1983년 설립됐다. 크론병, 궤양성 결장염 등 IBD를 중심으로 연구하고 있으며, 다기관 연구를 위해 프랑스뿐 아니라 벨기에, 스위스 대학병원이 센터로 등록돼 있다.
GETAID의 회장은 로랑 페이린 비룰레다. 그는 유럽염증성장질환학회(ECCO)의 회장이기도 하다. 로랑 페이린 비룰레 회장은 램시마SC 프랑스 출시 기자간담회에 참여해 프랑스 출시 의미 등에 대해 발표한 바 있다.
램시마SC는 2019년 11월 유럽에서 판매허가를 받은 바 있다. 당시 허가 적응증은 류마티스 관절염에 국한됐다. 이후 지난해 7월 IBD 적응증을 새롭게 획득했다.
프랑스에서는 올해 2월 출시됐다. 시장조사업체 아이큐비아에 따르면 램시마 성분인 ‘인플릭시맙’과 주요 자가면역질환 치료제인 ‘아달리무맙’, ‘에타너셉트’ 등 3개 성분의 시장 규모는 1조1000억원으로 추산되고 있다.
셀트리온 계열사 셀트리온헬스케어가 램시마IV와 램시마SC의 프랑스 유통을 담당하고 있다. 램시마IV는 올해 초 프랑스 최대 규모 대학병원 연합인 유니하(UNIHA) 입찰에서도 수주에 성공했다.
램시마IV와 램시마SC 교체 투여가 문제없다는 연구결과가 나온다면, 프랑스 내 처방 확대에 도움이 될 전망이다.
셀트리온헬스케어는 ‘램시마SC’ 출시로 기존 IV제형과 함께 환자 상태에 따른 맞춤형 치료가 가능한 듀얼 포뮬레이션(Dual formulation)의 강점이 동반상승 효과를 낼 것으로 보고 있다.
피하주사 제형은 환자가 집에서도 자가 주사가 가능하다. 때문에 신종 코로나바이러스 감염증(코로나19) 대유행 상황에서 병원을 자주 방문하지 않아도 된다는 장점도 있다.
셀트리온헬스케어 관계자는 “현재 독일, 영국, 프랑스, 스페인, 이탈리아, 네덜란드, 벨기에 등 유럽 주요 국가에서 출시를 마쳤다”고 설명했다.
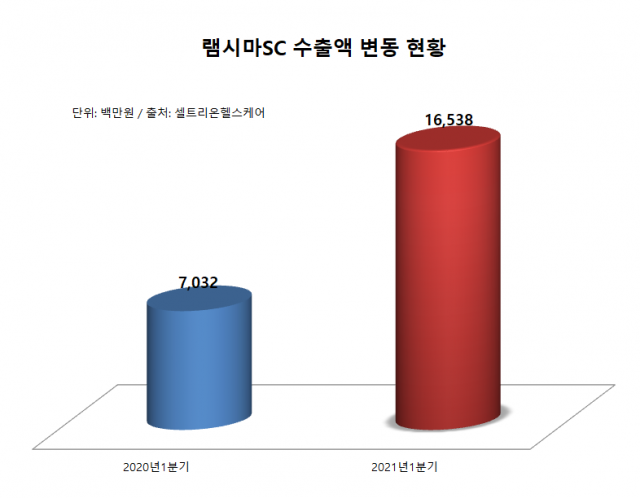
유럽 내 출시 국가가 늘면서 램시마SC 수출액은 지난해 1분기 70억3200만원에서 올해 1분기 165억3800만원으로 135.2% 증가했다.
[CEO스코어데일리 / 김윤선 기자 / yskk@ceoscore.co.kr]



![[현장을 가다] 아모레뷰티파크에서 탄생 100주년 서성환 선대회장의 '동백나무 정신'을 만나다](https://www.ceoscoredaily.com/photos/2024/03/22/2024032213414139276_m.jpg)
![[현장을 가다] “‘아리아’가 나를 살렸어”…SKT ‘AI 스피커’, 어르신 말동무 이자 ‘보디가드’로 활약](https://www.ceoscoredaily.com/photos/2024/04/01/2024040109491192497_m.jpg)
![[현장을 가다] ‘자동차 메카’에서 ‘전기차 허브’로…현대차 울산공장 가보니](https://www.ceoscoredaily.com/photos/2024/03/22/2024032216190656760_m.jpg)

![[그래픽] 롯데GRS 실적 추이](https://www.ceoscoredaily.com/photos/2024/04/26/2024042609264395390_m.jpg)
























































































![[24-03호]_500대기업 R&D 투자 현황](https://www.ceoscoredaily.com/photos/2024/04/17/2024041718513086340_m.jpg)

![[이달의 주식부호] 홍라희 여사 2위 탈환…곽동신 한미반도체 부회장 6위로 2계단↑](https://www.ceoscoredaily.com/photos/2024/04/03/2024040314314813956_m.jpg)



![[그래픽] 그레이트 컴퍼니 우수기업 리스트](https://www.ceoscoredaily.com/photos/2023/08/24/2023082410452781615_m.jpg)



댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.