임상시험 실시하는 총 7곳 실시기관 대상자 모집 시작
일부 실시기관 1차 대상자 모집 완료
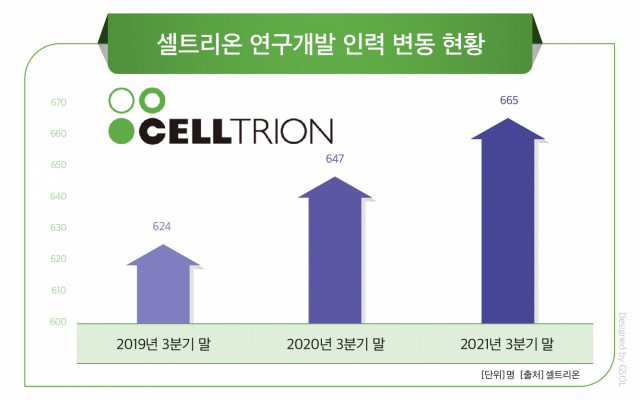
전체 직원 중 연구인력 비중 30.7%…개발 단계별로 담당 세분화
셀트리온(대표 기우성)이 최근 개발하기 시작한 ‘악템라(성분명 토실리주맙)’ 바이오시밀러 'CT-P47'의 임상시험에 속도를 내고 있다.
임상시험계획 승인을 받은 지 일주일도 되지 않아 대상자 모집에 돌입했다. 한 달도 지나지 않은 현재 1차 모집을 완료한 일부 기관도 있는 것으로 파악되고 있다.
27일 관련 업계에 따르면 셀트리온의 CT-P47의 국내 임상시험 1상 실시기관 총 7곳에서 모두 임상시험 대상자 모집에 돌입했다.
지난 12월6일 셀트리온은 CT-P47의 임상시험계획서를 승인 받은 바 있다. 승인을 받은 지 일주일도 되지 않아 일부 임상시험 실시기관에서 대상자 모집을 시작했고, 12월 넷째 주 기준으로 모든 기관이 대상자 모집을 하고 있다.
실시기관은 가천대길병원, 충북대병원, 전북대병원, 서울대병원, 분당서울대병원, 고려대구로병원, 인제대부산백병원 등이다.
이 중 모집을 일찍 시작한 일부 기관에서는 1차 모집을 완료한 것으로 알려졌다. 이들 기관에서 모집한 대상자들은 12월 말~1월 초엔 신체검사를 받을 예정이다.
임상시험 대상자(환자 및 건강인) 모집을 시작해야 본격적으로 임상에 ‘돌입’했다고 평가 받는다. 임상시험계획서 승인을 받고서 몇 개월이 지나야 대상자 모집을 시작하는 곳도 더러 있다. 대상자 모집이 늦어질수록 의약품 개발 기간은 늘어난다. 빠른 대상자 모집이 중요한 이유다.
셀트리온은 이번 국내 임상 1상 시험에서 건강한 시험대상자를 대상으로 악템라와 CT-47 투여한 후 약동학 및 안전성을 비교할 예정이다. 목표 대상자 수는 총 300명이다.
셀트리온은 국내 제약바이오 기업 중 임상시험을 빠르게 진행하는 곳으로 평가받고 있다.
일련의 개발 단계별로 일사불란하게 움직일 수 있도록 촘촘히 조직한 결과, 빠른 임상시험 진행이 가능한 것으로 분석되고 있다.
이 회사 연구개발 인력은 크게 △연구개발부문(생명공학연구본부, 신약연구본부, R&D QA) △제품개발부문(허가본부, 임상개발본부, 의학본부, 케미컬제품개발본부) △데이터사이언스본부 등 세 부문으로 나뉜다.
부문 산하 본부 내에서도 담당을 세세하게 나누었다. 한 예로 임상시험 기획이나 임상시험계획서 작성은 제품개발부문 산하 의학본부의 ‘클리니컬플래닝(Clinical Planning, 임상기획)’팀이 담당한다.
또 임상시험계획서가 승인 받은 후 임상시험 개시와 운영, 환자모집과 대행기관 관리는 제품개발부문 산하 임상개발본부의 ‘클리니컬오퍼레이션(Clinical Operation, 임상운영)’팀이 담당한다. 이들 팀도 다시 1담당, 2담당 등으로 나뉜다. 한 예로 임상운영팀은 1담당(27명), 2담당(28명), 3담당(28명)으로 세분화 돼 있다.
올해 3분기 말 셀트리온 연구개발 인력은 총 665명이다. 전체 직원 2169명 중 30.7%가 연구개발 인력에 해당한다. 연구개발 인력의 부문별 비중은 △연구개발부문 32.2%(214명) △제품개발부문 57.0%(379명) △데이터사이언스센터본부 10.8%(72명) 등이다. 임상시험 진행, 허가 등 의약품 상업화와 밀접한 역할을 맡은 제품개발부문 인력이 제일 많다.
셀트리온 측은 “2030년까지 매년 1개 이상의 바이오시밀러 제품 허가를 완료한다는 계획”이라고 설명했다.
[CEO스코어데일리 / 김윤선 기자 / yskk@ceoscore.co.kr]




![[4·10 총선] 野, 금융공약 ‘생계비계좌’ 도입…비트코인 현물 ETF 허용 추진](https://www.ceoscoredaily.com/photos/2024/04/05/2024040517040346372_m.jpg)
![[4·10 총선] 與, 금융분야 ‘금투세 폐지’ 드라이브…중도상환수수료 개선 공약](https://www.ceoscoredaily.com/photos/2024/04/04/2024040417544322677_m.jpg)
![[2024 전망] 유통업계, ‘불황형 소비’ 속 기회 모색…“업체간 생존경쟁 치열할 듯”](https://www.ceoscoredaily.com/photos/2024/01/04/2024010417183989377_m.jpg)

![[그래픽] 넷마블의 5월 신작 MMORPG ‘레이븐2’](https://www.ceoscoredaily.com/photos/2024/04/19/2024041909194548328_m.jpg)
























































































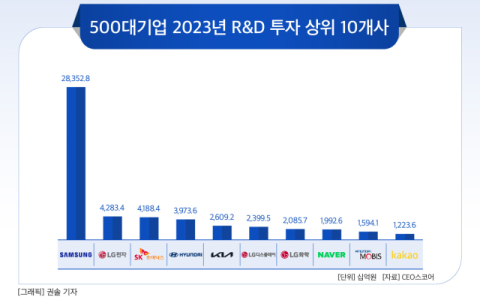
![[24-03호]_500대기업 R&D 투자 현황](https://www.ceoscoredaily.com/photos/2024/04/17/2024041718513086340_m.jpg)

![[이달의 주식부호] 홍라희 여사 2위 탈환…곽동신 한미반도체 부회장 6위로 2계단↑](https://www.ceoscoredaily.com/photos/2024/04/03/2024040314314813956_m.jpg)



![[그래픽] 그레이트 컴퍼니 우수기업 리스트](https://www.ceoscoredaily.com/photos/2023/08/24/2023082410452781615_m.jpg)



댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.