2016년 개발, 내년 출시 목표…기존 제품 대비 생산 수율 향상
메디톡스 계열사 메디톡스코리아(대표 주희석·오경석)가 개발하고 있는 신규 보툴리눔톡신 제제의 임상 3상 환자 모집에 본격 돌입했다. 이 제품은 회사의 기존 동결 건조 제형 제품과 달리 새로운 제조공정을 적용한 원액을 사용했으며 내년 출시가 목표다.
29일 관련 업계에 따르면 메디톡스코리아의 보툴리눔톡신 제제 ‘MBA-P01'가 국내에서 임상 3상 시험을 위한 환자 모집에 최근 돌입했다.
앞서 메디톡스코리아는 지난 6월23일 국내 식품의약품안전처로부터 MBA-P01의 임상 3상 시험계획서를 승인 받은 바 있다. 이 시험에선 중등증 및 중증의 미간 주름 개선이 필요한 환자를 대상으로 MBA-P01을 투여한 후 유효성과 안전성 등을 확인하게 된다. 총 목표 대상자 수는 318명이며, 대조약은 앨러간의 ‘보톡스주’다.
메디톡스는 2016년 MBA-P01의 개발에 착수했다. 이후 2018년 3월 식약처로부터 임상 1상시험계획을 승인받고 시험을 완료했으며, 2상은 호주에서 진행했다.
메디톡스는 기존에 국내에서 △메디톡신 △이노톡스 △코어톡스 등 3가지 보툴리눔톡신 제제의 허가를 획득했다. 하지만 무허가 원액 사용, 안정성 시험 자료 조작 제출 등의 혐의로 메디톡신과 코어톡스는 지난해 11월 품목허가 취소 처분을 받았다. 올해 1월 식약처는 코어톡스에 대해서도 품목허가 취소 처분을 내렸다.
대전지방행정법원이 올해 초 메디톡스가 대전지방식약청장을 상대로 제기한 품목허가 취소 처분 등에 대한 집행정지 신청에 대해 효력정지 결정을 내리면서 보툴리눔톡신 제제들을 다시 판매할 수 있게 됐다. 하지만 매출 회복에는 다소 시간이 걸릴 것으로 예상된다.
메디톡스는 MBA-P01과 같은 신규 보툴리눔톡신 제제 개발을 빠르게 완료해 매출 확대를 꾀할 것으로 전망된다.
회사 측에 따르면 MBA-P01은 동결 건조 제형의 기존 보툴리눔톡신 제제와 달리 새로운 제조공정을 적용한 원액을 사용하고 최신 기술을 적용, 생산 수율과 품질을 향상시켰다. 또 제조과정 중 보툴리눔 균주 배양 단계에서 사용되는 동물 유래 물질 단백질 대신 비동물성 원료 배지를 사용한 것이 특징이다.
메디톡스코리아 관계자는 “차세대 보툴리눔 톡신 제제인 ‘MBA-P01’은 보다 향상된 품질로 톡신 시장을 재편할 수 있는 무한한 잠재력을 가진 의약품”이라면서 “임상 3상을 차질 없이 진행해 내년 출시 목표를 달성하고, 해외 진출을 위한 기술수출 등의 논의도 함께 진행할 것”이라고 말했다.
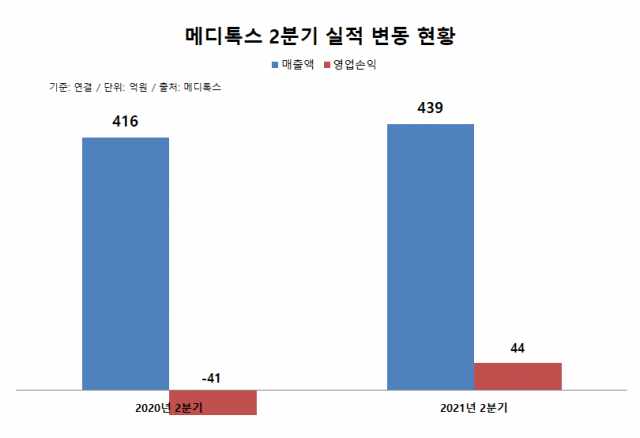
메디톡스는 올해 2분기 연결 기준 매출액 439억원, 영업이익 44억원을 기록했다. 매출액은 지난해 동기 대비 5.5% 증가했으며 영업손익은 흑자전환했다. 영업손익은 2019년 3분기 이후 7분기 만의 흑자전환이다. 회사 측은 매출 증가 이유로 △보툴리눔톡신 제제 매출 회복 △미국 ITC 소송에서 승소 이후 비용 부담 해소 △ITC 소송 이후 체결한 계약으로 합의금 반영 등을 꼽았다.
[CEO스코어데일리 / 김윤선 기자 / yskk@ceoscore.co.kr]




![[현장을 가다] “‘아리아’가 나를 살렸어”…SKT ‘AI 스피커’, 어르신 말동무 이자 ‘보디가드’로 활약](https://www.ceoscoredaily.com/photos/2024/04/01/2024040109491192497_m.jpg)
![[현장을 가다] ‘자동차 메카’에서 ‘전기차 허브’로…현대차 울산공장 가보니](https://www.ceoscoredaily.com/photos/2024/03/22/2024032216190656760_m.jpg)
![[4·10 총선] 野, 금융공약 ‘생계비계좌’ 도입…비트코인 현물 ETF 허용 추진](https://www.ceoscoredaily.com/photos/2024/04/05/2024040517040346372_m.jpg)

![[그래픽] 2022-2023년 6개 카드사 리스자산 추이](https://www.ceoscoredaily.com/photos/2024/04/25/2024042509404783573_m.jpg)
























































































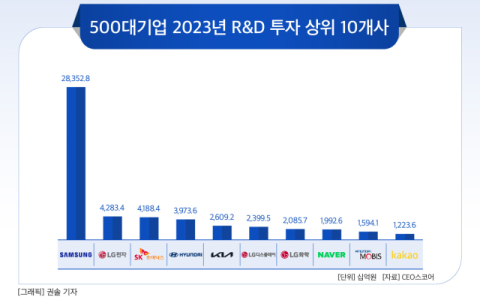
![[24-03호]_500대기업 R&D 투자 현황](https://www.ceoscoredaily.com/photos/2024/04/17/2024041718513086340_m.jpg)

![[이달의 주식부호] 홍라희 여사 2위 탈환…곽동신 한미반도체 부회장 6위로 2계단↑](https://www.ceoscoredaily.com/photos/2024/04/03/2024040314314813956_m.jpg)



![[그래픽] 그레이트 컴퍼니 우수기업 리스트](https://www.ceoscoredaily.com/photos/2023/08/24/2023082410452781615_m.jpg)



댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.