최대 시장 미국 진출 기대...1분기 중 허가신청서 제출 계획
첫 적응증 ‘미간 주름 개선’ 유력
휴젤(대표집행임원 손지훈)의 보툴리눔톡신 제제가 미국 내 주요 임상들을 최근 속속 완료하고 있다. 임상시험 확인 대상 효능이 ‘미간 주름 개선’인 만큼 첫 적응증도 이와 같을 것으로 예상된다.
8일 관련 업계에 따르면 휴젤의 미국 및 유럽 파트너사 크로마파마(CROMA-PHARMA GmbH, 이하 크로마)가 지난해 12월부터 현재까지 2건의 미국 내 임상시험을 종료했다.
먼저 지난해 12월 말 휴젤의 보툴리눔톡신A 제제의 미간 주름 개선 효과와 안전성을 확인하는 임상 3상 시험을 종료했다. 2019년 4월 시작된 이 시험은 총 355명의 대상자가 실제 등록됐다. 대조 위약은 식염수로 설정했다.
이어 지난달 또 한 건의 임상시험이 종료됐다. 이 시험은 임상 2상 시험으로, 미국뿐 아니라 캐나다와 유럽(오스트리아)에서도 동시 진행됐다. 2019년 12월 시작된 이 시험은 총 200명을 대상으로 했다. 앞선 임상 3상과 동일하게 미간 주름 개선 효과를 확인했지만, 대조약을 식염수가 아닌 엘러간의 미용 시장용 보툴리눔톡신 제제인 ‘보톡스 코스메틱’으로 설정했다.
휴젤 측은 올해 1분기 중 미국 식품의약국(FDA)에 자사 보툴리눔톡신 제제의 허가를 신청한다는 계획이다.
허가 신청 시 적응증은 ‘미간 주름 개선’이 유력해보인다. 앞서 휴젤은 지난해 10월 중국 국가약품감독관리국(NMPA)으로부터 보툴리눔톡신 제제 레티보(국내명 보툴렉스)의 판매 허가 승인을 받은 바 있다. 허가 적응증은 미간 주름 개선이다.
유럽의약품청(EMA)엔 지난해 6월 품목허가를 신청했다. 올해 상반기 안으로 허가 여부가 판가름 날 전망이다.
휴젤 보툴렉스는 2009년 3월 국내 식품의약품안전처로부터 100유닛 허가를 받은 바 있다. 미용 적응증뿐 아니라 양성 본태성 눈꺼풀 경련의 치료 등 치료 목적 적응증도 다수 획득했다.
미국 진출에 성공한다면 먼저 미용 시장 우선 공략 후 차츰 영역을 넓힐 것으로 예상된다. 가격은 후발주자인만큼 엘러간 등 주요 기업 대비 낮은 가격을 책정할 가능성이 높다.
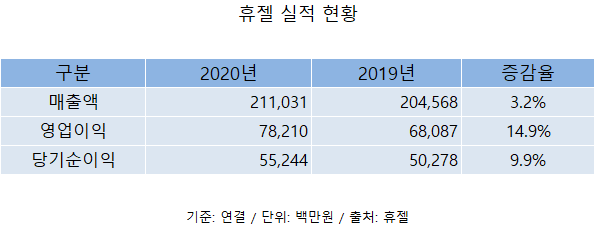
휴젤은 지난해 메디톡스 등 경쟁 업체의 부진 속 수혜를 입었다. 이 회사는 지난해 연결 기준 매출액 2110억3075만원, 영업이익 782억958만원, 당기순이익 552억4446만원을 기록했다. 전년비 매출액은 3.2% 증가해 사상 최대치다. 영업이익은 전년비 14.9% 증가했고 영업이익률은 37.1%를 기록했다.
[CEO스코어데일리 / 김윤선 기자 / yskk@ceoscore.co.kr]



![[4·10 총선] 野, 금융공약 ‘생계비계좌’ 도입…비트코인 현물 ETF 허용 추진](https://www.ceoscoredaily.com/photos/2024/04/05/2024040517040346372_m.jpg)
![[4·10 총선] 與, 금융분야 ‘금투세 폐지’ 드라이브…중도상환수수료 개선 공약](https://www.ceoscoredaily.com/photos/2024/04/04/2024040417544322677_m.jpg)
![[2024 전망] 유통업계, ‘불황형 소비’ 속 기회 모색…“업체간 생존경쟁 치열할 듯”](https://www.ceoscoredaily.com/photos/2024/01/04/2024010417183989377_m.jpg)

![[그래픽] 넷마블의 5월 신작 MMORPG ‘레이븐2’](https://www.ceoscoredaily.com/photos/2024/04/19/2024041909194548328_m.jpg)
























































































![[24-03호]_500대기업 R&D 투자 현황](https://www.ceoscoredaily.com/photos/2024/04/17/2024041718513086340_m.jpg)

![[이달의 주식부호] 홍라희 여사 2위 탈환…곽동신 한미반도체 부회장 6위로 2계단↑](https://www.ceoscoredaily.com/photos/2024/04/03/2024040314314813956_m.jpg)



![[그래픽] 그레이트 컴퍼니 우수기업 리스트](https://www.ceoscoredaily.com/photos/2023/08/24/2023082410452781615_m.jpg)



댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.